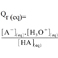espace pédagogique > disciplines du second degré > physique chimie > enseigner > expériences et manipulations
réaction acide-base et quotient réactionnel
mis à jour le 02/11/2019
déterminer l'état final d'un système et de comparer le quotient réactionnel à la constante d'équilibre, dans le cas de la réaction de dissociation d'un acide dans l'eau, par conductimétrie.
mots clés : chimie, CBSV, état final, quotient, réactionnel, constante, équilibre, réaction, acide-base
![Accueil [legende-image]1424145810101[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/accueil-pc_1560080380675-jpg?ID_FICHE=545356) |
Accueil | ![numérique [legende-image]1424145810107[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/numerique_1560081272508-jpg?ID_FICHE=545356) |
Numérique | ![collège [legende-image]1424145810109[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/college-2016_1560081636373-jpg?ID_FICHE=545356) |
Collège | ![enseigner [legende-image]1424145810102[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/rechercher-des-ressources-pedagogiques_1560080503885-jpg?ID_FICHE=545356) |
Enseigner | ![se former [legende-image]1424145810108[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/carre-jaune_1560081466520-jpg?ID_FICHE=545356) |
Se former | ![s'informer [legende-image]1424145810103[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/les-dernieres-actualites_1560080612518-jpg?ID_FICHE=545356) |
S'informer | ![lycée [legende-image]1424145810098[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/nouveau-lycee-2019_1560079683815-jpg?ID_FICHE=147469) |
Lycée |
 |
 |
 |
![ressources 2nde [legende-image]1424145819776[/legende-image]](/medias/photo/screenhunter-713-oct-21-17-32_1571671942522-jpg) |
![ressources 1ère [legende-image]1424145819779[/legende-image]](/medias/photo/screenhunter-715-oct-21-17-36_1571672254646-jpg) |
![ressources Terminale [legende-image]1424145819780[/legende-image]](/medias/photo/screenhunter-716-oct-21-17-52_1571673229637-jpg?ID_FICHE=553319) |
![des sites de ressources [legende-image]1424145819708[/legende-image]](https://www.pedagogie.ac-nantes.fr/medias/photo/logositeinternet_1571594339938-png) |
 |
|||||||
| Accueil Lycée |
programmes 2019 |
nouvelles séquences lycée |
ressources en 2nde |
ressources en 1ère |
ressources en terminale |
sites de ressources |
Les élèves doivent d'abord réaliser deux dilutions à partir d'une solution mère d'acide méthanoïque ou d'acide éthanoïque, puis mesurer la conductivité de chacune des 3 solutions. Ils doivent ensuite exprimer le quotient de réaction à l'équilibre en fonction de la concentration en ions oxonium dans l'état d'équilibre. Puis, il s'agit d'exploiter les mesures conductimétriques pour en déduire les concentrations molaires des espèces chimiques présentes en solution, à l'équilibre ; et enfin de déterminer le quotient réactionnel. Une moyenne des différentes valeurs obtenues pour Qr par les différents groupes pourra être faite, ainsi qu'une détermination de l'incertitude de répétabilité.
L'activité se termine par une comparaison du quotient réactionnel à la constante d'équilibre.
(des documents sont à disposition).
Travaux Pratiques - activité expérimentale.
Objectifs :
- Déterminer l'état final d'un système
- Comparer le quotient réactionnel Qr à la constante d'équilibre K
Prérequis :
- Savoir réaliser des mesures conductimétriques (réalisation en SPCL, en 1ère de titrages conductimétriques et en terminale : concevoir et mettre en œuvre un protocole pour comparer qualitativement des conductivités molaires ioniques d'anions et de cations)
Documents à disposition :
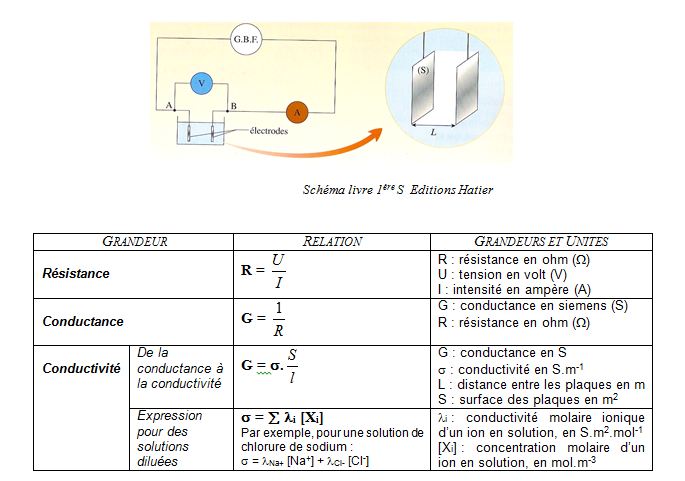
- Document 1 : Rappels de conductimétrie
- Document 2 : Quelques données
- Acide méthanoïque / ion méthanoate : HCOOH(aq) / HCOO-(aq)
- Acide éthanoïque / ion éthanoate : CH3COOH(aq) / CH3COO-(aq)
- Conductivités molaires ioniques à 25 °C :
(H3O+) : 35,0 x 10-3 S.m2.mol-1 ;
(CH3COO-) : 4,09 x 10-3 S.m2.mol-1 ;
(HCOO-) : 5,46 x 10-3 S.m2.mol-1
Matériel et solutions à disposition :
- fiole jaugée de 50 mL
- pipettes jaugées de 5 mL, 10 mL et 20 mL
- bécher de 150 mL
- conductimètre
- solution aqueuse d'acide méthanoïque ou d'acide éthanoïque à CA = 0,10 mol.L-1
- eau distillée
Travail à réaliser :
Répartition du travail entre les binômes.
Chaque binôme travaille sur trois solutions d'un même acide de concentrations différentes.
| N° binômes | Nature des solutions | Concentrations c en mol.L-1 |
| Binômes 1, 2, 3, 4 | Acide éthanoïque | 0,10 ; 0,02 ; 0,01 |
| Binômes 5, 6, 7, 8 | Acide méthanoïque | 0,10 ; 0,02 ; 0,01 |
- Mise en œuvre du protocole et réalisation des mesures
- A partir de la solution d'acide méthanoïque ou d'acide éthanoïque à votre disposition, proposer un protocole pour préparer les deux solutions filles.
- Mettre en œuvre le protocole.
- Mesurer la conductivité de chacune des trois solutions.
- Exploitation des résultats obtenus
- On dispose d'un volume V de solution aqueuse d'un acide HA de concentration molaire apportée C. La réaction de cet acide HA sur l'eau n'est pas totale.
- Après avoir écrit l'équation de la réaction et dressé un tableau d'avancement, exprimer le quotient de réaction à l'équilibre, en fonction de la concentration en ion oxonium dans l'état d'équilibre [H3O+]eq et de C.
- Exprimer la conductivité sigma de la solution, et en déduire l'expression de la concentration en ions oxonium à l'équilibre, en fonction de sigma et des conductivités molaires ioniques.
- En déduire la valeur du quotient de réaction à l'équilibre, pour les 3 solutions.
- Déterminer l'état final du système.
- Validation des résultats
- Mettre en commun l'ensemble des résultats obtenus par les n groupes de la classe, puis calculer la valeur moyenne Qr (moy) après suppression éventuelle de résultats manifestement aberrants.
- Déterminer l'incertitude de répétabilité U(Qr), puis présenter le résultat sous la forme Qr (moy) ± U(Qr).
Vous pouvez vous aider de la fiche sur les incertitudes de mesures. - Comparer avec la constante d'acidité donnée dans les tables à 25°C
Pour le couple HCOOH / HCOO- on trouve dans les tables Ka = 1,8.10-4
Pour le couple CH3COOH / CH3COO- on trouve dans les tables Ka = 1,8.10-5
Cette valeur appartient-elle à l'intervalle de confiance déterminé expérimentalement ?
Conclure.
Coups de pouce possibles :
1. Expression de Qr, eq en fonction de la concentration en ion oxonium dans l'état d'équilibre [H3O+]eq
- Écrire l'équation de la réaction mise en jeu.
- Dresser un tableau d'évolution des espèces chimiques au cours de la transformation chimique de AH dans l'eau. On appellera x l'avancement de réaction et xeq l'avancement final (ou à l'équilibre).
- Ajouter une ligne au tableau en considérant la réaction comme totale. Dans cette hypothèse, exprimer l'avancement maximal xmax en fonction de c et v.
- Définir le quotient de réaction Qr, eq à l'équilibre. Exprimer le quotient de réaction Qr, eq à l'équilibre, en fonction de [H3O+]eq et de c.
2. Comment déterminer Qr, eq par conductimétrie ?
- Exprimer la conductivité de la solution de HA, en fonction des conductivités molaires ioniques des ions A- et H3O+ présents et de [H3O+]eq.
- Comment déterminer les concentrations molaires effectives en ions oxonium, [H3O+]eq, et en ions A-, [A-]eq à partir de la mesure de la conductivité ?
- Comment déterminer la concentration en acide HA à l'équilibre à l'aide du tableau d'avancement ? L'exprimer en fonction de [H3O+]eq.
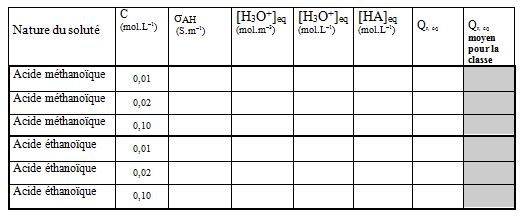
3. Compléter le tableau :
information(s) pédagogique(s)
niveau : Terminale STL
type pédagogique : scénario, séquence, travaux pratiques
public visé : élève
contexte d'usage : laboratoire
référence aux programmes :
BO spécial n°8 du 13 octobre 2011 - Programme d'enseignement de chimie-biochimie-sciences du vivant
Classe terminale de la série technologique STL
Thème 2 : Les systèmes vivants échangent de la matière et de l'énergie > Les systèmes vivants assurent leur activité et maintiennent leur intégrité en utilisant des voies métaboliques variées
Capacités :
- Mettre en œuvre une activité expérimentale pour déterminer l'état final d'un système, dans le cas d'une réaction acide-base
- Exprimer le quotient réactionnel Qr et le comparer à la constante d'équilibre K(T), par exemple KA pour la réaction de dissociation d'un acide dans l'eau.
fichier joint
information(s) technique(s) : Fichier modifiable au format . doc
taille : 652 kio ;
physique chimie - Rectorat de l'Académie de Nantes

 s'identifier
s'identifier
 portail personnel ETNA
portail personnel ETNA